- Argomento
- Sanità
Leucemia Mieloide Acuta: la nanomedicina è già parte della soluzione
Il progetto LEUCITI, grazie alle tecniche di nanomedicina, vuole rendere più efficaci i farmaci per la cura dei tumori del sangue veicolandoli all'interno delle cellule tumorali. I dati raccolti nei test in vitro sono molto incoraggianti.
Autore Luigi PanzaDaniela Imperio
Data di pubblicazione
Il progetto Leuciti (sito Web), coordinato dall'Università del Piemonte Orientale nell'ambito del programma dei progetti di cooperazione Italia-Svizzera INTERREG, nasce con lo scopo di dar spazio alla ricerca traslazionale coinvolgendo diversi partners, accademici, di ricerca sanitaria e industriali. Se in passato infatti ci si occupava quasi esclusivamente degli aspetti scientifici, adesso si tiene conto anche delle necessità del mercato, della produzione e degli aspetti regolatori legati allo sviluppo di un nuovo potenziale farmaco. In particolare, Leuciti ha consentito lo sviluppo di un’importante collaborazione con IRB (Istituto di Ricerca in Biomedicina con sede a Bellinzona), leader mondiale per lo sviluppo e la caratterizzazione di anticorpi, con la Fondazione Tettamanti di Monza, leader nella ricerca e nella terapia della leucemia nei bambini, con il gruppo di ricerca del Prof. Mauro Fasano del Dipartimento di Scienza e Alta Tecnologia dell’Università dell’Insubria e con Cerbios-Pharma SA, importante azienda farmaceutica ticinese. Il topic di questo progetto riguarda il trattamento della Leucemia mieloide acuta (AML), una patologia delle cellule del midollo osseo causata da anomalie a carico di cellule ematopoietiche quando si trovano nello stadio di precursori immaturi. Normalmente, il midollo osseo è la nostra fabbrica che produce cellule staminali del sangue che maturano nel tempo diventando cellule del sangue mature. La leucemogenesi causa un blocco della differenziazione cellulare e un’aumentata proliferazione della cellula immatura che prende il nome di blasto, ovvero una cellula con caratteristiche morfologiche atipiche.
Progetto LEUCITI Tutti i dettagli del progetto LEUCITI sono disponibili sul sito progetti.interreg-italiasvizzera.eu
AML è la patologia oncologica più frequente in età pediatrica e rappresenta circa il 40% di tutte le neoplasie; ogni anno, in Italia, si ammalano circa 70 bambini. La malattia presenta un picco entro il primo anno di vita, e aumenta nuovamente fra i 10-14 anni di età. Esistono diverse tipologie di trattamento: chemioterapia, radioterapia, utilizzo di cellule staminali, targeted- terapia oppure l’utilizzo di altri farmaci ancora in studio.
AML è la patologia oncologica più frequente in età pediatrica e rappresenta circa il 40% di tutte le neoplasie.
La citarabina e la daunorubicina rappresentano ad oggi la combinazione di farmaci chemioterapici di scelta per il trattamento della AML ma hanno elevata tossicità con prognosi nefasta per pazienti deboli, tipicamente bambini e adulti sopra i 55 anni. La polichemioterapia è, di fatto, in grado di ridurre la malattia, a cui segue una terapia di consolidamento. Tuttavia durante il trattamento polichemioterapico, i pazienti vanno incontro a diverse problematiche, in primis gli effetti collaterali, mal sopportati dalla maggioranza dei malati, a cui si somma un’alta percentuale di recidiva. L’approccio che abbiamo seguito ha previsto la possibilità di indirizzare i farmaci chemioterapici contro le cellule tumorali salvaguardando, per quanto possibile, le cellule sane (targeted delivery) andando a bersagliare le cellule staminali leucemiche.
Una strategia comunemente utilizzata in ambito farmacologico per ridurre gli effetti collaterali dei farmaci è quella di inglobare il farmaco all’interno di una gabbia, ovvero una struttura molecolare in grado di mantenere al suo interno il composto fino al raggiungimento del target specifico. Abbiamo, pertanto, prodotto un liposoma, ovvero una vescicola formata da un doppio strato di fosfolipidi, che può avere dimensioni variabili nell’ordine dei nanometri, in cui racchiudere il farmaco al fine di essere veicolato e rilasciato solo dopo essere stato internalizzato nella cellula tumorale. Per garantire la selettività, sulla superficie esterna del liposoma è stato legato un anticorpo specifico in grado di riconoscere le cellule staminali leucemiche, andando a generare un immunoliposoma. Per produrre il liposoma abbiamo lavorato sulla composizione dei singoli fosfolipidi, siamo riusciti a produrre una vescicola sensibile al pH, ovvero stabile a pH fisiologico ma instabile quando, dopo essere internalizzata, entra negli endosomi dove trova un pH acido (Fig 1).
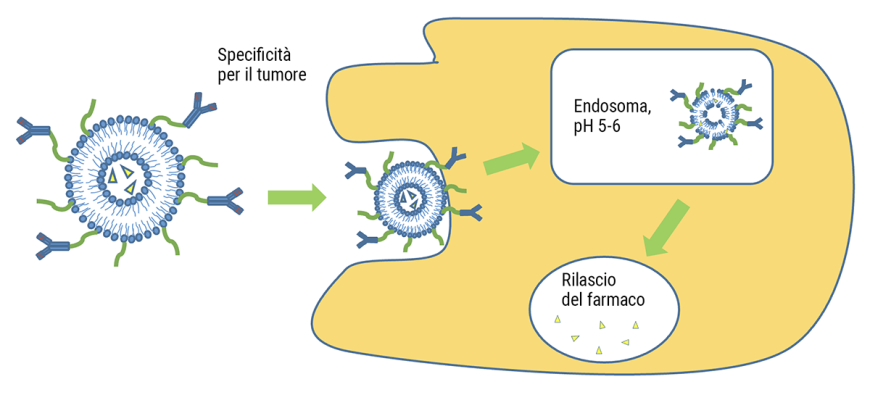
Figura 1 Fig. 1. I ricercatori hanno "creato" una vescicola sensibile al pH, ovvero stabile a pH fisiologico ma instabile quando, dopo essere internalizzata, entra negli endosomi dove trova un pH acido.
Quello che si osserva è una destabilizzazione della struttura della parete della vescicola che causa il rilascio del farmaco antitumorale. La struttura liposomiale prodotta si è dimostrata essere stabile e con dimensioni riproducibili. L'immunoliposoma è stato quindi testato su cellule THP-1 (linea cellulare monocitica umana derivata da un paziente con leucemia monocitica acuta) e sulle cellule CALL-4 (B cell leukemia precursor), dove è stata osservata una maggior mortalità di queste ultime rispetto alle prime.
Questo importante risultato trovato in vitro dimostra come la nanomedicina “di precisione” possa essere un valido aiuto per una terapia specifica verso un target tumorale. Inoltre composti liposoma/farmaco sono già presenti sul mercato ma non sono in grado di indirizzare il farmaco selettivamente contro le cellule tumorali. Gli anticorpi possono svolgere questo ruolo ma non vi è alcun prodotto simile in commercio. I test finora effettuati sono un punto di partenza per sviluppare una terapia ad hoc. Quello che ci aspettiamo in futuro è una valutazione su campioni sanguigni di pazienti malati. Una terapia targettante potrebbe infatti portare a una maggiore selettività di azione del farmaco garantendo una riduzione degli effetti collaterali e una miglior tolleranza alla terapia. Anche se la strada verso l’applicazione pratica non è breve, i dati preliminari raccolti sono incoraggianti e ci rendono fiduciosi per il futuro del progetto.
Accanto agli aspetti strettamente scientifici, il progetto ha anche favorito un’interazione e una positiva collaborazione tra enti di ricerca, e tra questi e un’azienda farmaceutica, collaborazione che speriamo possa continuare in maniera proficua anche in futuro. Tutto questo è stato reso possibile grazie alla cornice del programma INTERREG Italia-Svizzera che ha finanziato il progetto supportando la ricerca e il personale coinvolto. Grazie a un finanziamento durato diciotto mesi abbiamo posto le basi di ricerca per uno sviluppo futuro tutto da scrivere, a cominciare dalla divulgazione dei suoi contenuti nelle scuole e presso i cittadini.
Ultima modifica 10 Novembre 2022
Leggi anche
Scoperto il ruolo della proteina VDBP nell’atrofia muscolare: una nuova speranza contro la cachessia tumorale
- Argomento
- Sanità
Data di pubblicazione
16 Aprile 2026
Aging in progress: dalla ricerca di base all'applicazione sul territorio
- Argomento
- Sanità
Autore Carmela Rinaldi
Data di pubblicazione
31 Ottobre 2024

La medicina del futuro tra convenzione e tradizione. Il dialogo tra le università e i ponti da costruire tra Occidente e Oriente
- Argomento
- Sanità
Autore Ciro Isidoro
Data di pubblicazione
27 Agosto 2024

A ognuno il suo vaccino
- Argomento
- Sanità
Autore Marisa Gariglio
Data di pubblicazione
11 Febbraio 2022
Batteri e probiotici. I nostri nuovi alleati contro il diabete del futuro
- Argomento
- Sanità
Autore Flavia Prodam Marina Caputo
Data di pubblicazione
21 Dicembre 2021

In Sierra Leone nasce il primo servizio nazionale di emergenza pre-ospedaliera
- Argomento
- Sanità
Autore Marta Caviglia
Data di pubblicazione
21 Novembre 2021
